胰腺癌基因靶向治疗 大盘点:胰腺癌的基因和靶向治疗(综述)
(原标题:胰腺癌基因靶向治疗 大盘点:胰腺癌的基因和靶向治疗(综述))
NCI 和 SEER 的数据显现胰腺癌 5 年生计只需 5-6%,大多数患者确诊时都已是开展期,区域性和远处搬运分别为 27% 和 53%。胰腺癌医治方面最近也没有突破性开展,含吉西他滨的医治和手术是近 10 余年来的规范医治,无论是用作新辅佐仍是辅佐化疗,化疗挑选很有限。美国 Frank 博士在 Canlet 杂志上介绍了个体化基因组医学在胰腺癌医治上的使用。
人类基因组计划(HGP)自 1990 年发动,于 2003 年提前完结,判定了大约 30 亿碱基对和大约 24,500 基因,可是直至 2007 年经过 Sanger 测序技能才完结人类基因测序。1 年后科学家选用快速测序 454 技能检测基因组,花费仅为传统测序费用的百分之一,历时 2 个月完结。新的测序技能和巨大的数据信息,促进「个体化基因组医学」的开展。
个体化基因组医学选用基因组信息进步确诊、辅导分子和基因医治挑选,医生经过查看高危患者癌症相关基因改动,如高危患乳腺癌患者查看 BRCA 基因,来辅导确诊与医治。现代技能答应直接芯片剖析唾液标本中的 DNA,该技能中心是单核苷酸多态性(SNPs)。SNPs 约占全 DNA 改动的 90%,与免疫组化联合有助于判定恶性疾病中蛋白表达与功用反常,特别合适用胰腺癌。
胰腺癌异质性很强,遗传学标志包含全基因组不稳定性,如骤变、易位和刺进/缺失、非整倍体。全基因组剖析显现,12 个中心信号途径皆有遗传学改动。最常见遗传学改动包含 DNA 仿制,KRAS、TGF-β、凋亡和细胞周期途径改动。引起林奇综合征的 MMR 骤变,引起遗传性乳腺-卵巢癌的 BRCA 骤变,在胰腺癌特别是宗族性胰腺癌中约占 5–10%。
胰腺肿瘤的遗传学改动能使得医生清晰:(1)肿瘤对化疗、放疗或是手术的医治反响;(2)细化医治,如新辅佐、辅佐和基因医治;(3)有用的药物使用办法。这些信息在临床上很重要,能够添加效果、下降毒性、改进患者的日子质量。胰腺癌十分简单呈现多药耐药,经过基因组学信息能够取得优化医治的相关信息,还能够猜测预后、削减不必要的医治。
胰腺癌标本能够经过如下手法获取:手术活检、内镜超声指引的细针抽吸(EUS-FNA)或循环中的肿瘤细胞(CTCs)。手术切除胰腺癌仍是活检金规范,而侵袭性较小的办法如 EUS-FNA 正在推行。可是 FNA 抽吸细胞难于在良性胰腺疾病中辨别恶性危害,如缓慢胰腺炎具有胰腺癌的细胞形状特征。
CTCs 来自原发或搬运方位的肿瘤,能够由外周血别离取得,是潜在的胰腺癌标志。最近选用深度测序血清标本中 KRAS 骤变状况,Yu 等建立了便利快速的办法查看 KRAS 骤变,灵敏性 87.5%,精确性 92.9%,当肿瘤标本无法取得时这或许是特别有价值的一种检测办法,因为要改进胰腺癌确诊或前期确诊需求新的分子或遗传学标志。
胰腺癌的基因组学
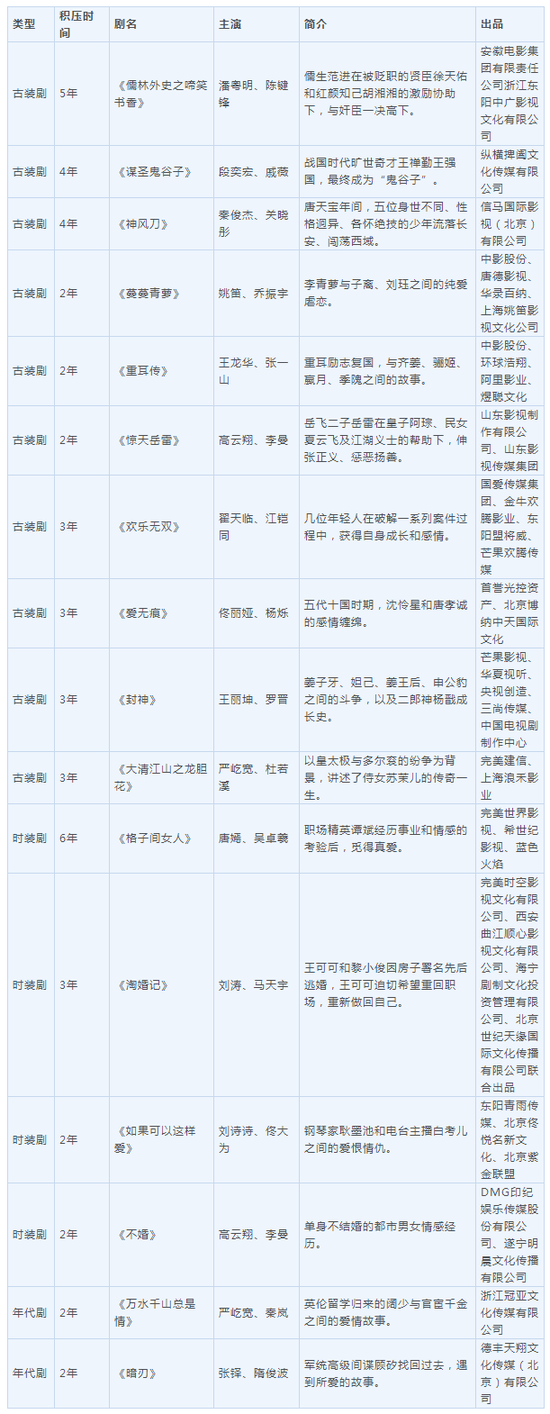
对胰腺癌开展和其遗传学改动之间的相关已有很深入的知道。2008 年 24 例胰腺癌全外显子组测序显现,均匀 63 个基因改动,多为点骤变,KRAS、CDKN2A、TP53 和 SMAD4 基因骤变最常见。Biankin 对 142 例 I 或 II 期术前胰腺癌基因组测序,判定了 16 个显着的骤变基因,包含 ATM 和 MLL3。其它陈述的基因有 BRCA1、PDX-1 和 SLC39A4。胰腺癌中要害基因总结见表 1。
表 1 胰腺癌的基因组学
KRAS 骤变存在于 90% 以上的侵袭性胰腺癌,与胰腺上皮内肿瘤(PanINs)开展为胰腺癌有关。KRAS 是原癌基因,一旦有点骤变活化,就能招募活化成长因子和受体信号,发作恶性转化;EGFR 具有促进肿瘤细胞成长的效果,是 KRAS 的上游基因。
结肠癌中假如 KRAS 活化,则靶向 EGFR 的药物无效,所以抗 EGFR 医治之前进行遗传学查看十分必要。经过粪便标本和实时甲基化特异性多聚酶链反响(MSP)检测 KRAS 或许会成为胰腺癌的一种检测办法。此外血浆 DNA 测序或许为了解癌症发作、前期确诊供给新的知道,EUS-FNA 答应医日子检胰腺癌以进一步对 KRAS 测序。
从 PanINs 开展到胰腺癌的进程中,CDKN2A 基因的缺失能够导致肿瘤按捺基因 P16 表达下调,在 86-95% 的发出胰腺癌中 P16 功用缺失发作在疾病前期。免疫组化显现淋巴侵略和短少 P16 表达之间存在显着的相关性。P16 能按捺细胞增殖,骤变后参加多肿人类癌症的发作开展。
P53 在 PanINs 开展到胰腺癌的进程中也常常发作骤变,它参加细胞周期捕获、活化 DNA、发动凋亡等进程。SMAD4/DPC4 肿瘤按捺基因是晚发事情,它参加 TGF-β介导的细胞成长调理,其缺失常常发作于搬运性疾病,下降总生计(OS)。
BRCA1/2 是 PanINs 开展到胰腺癌进程中的晚期事情,它参加 DNA 修正。体外数据显现 BRCA2 有缺点的人类胰腺癌细胞株对 DNA 危害高灵敏,如 PARP 按捺剂。PARP 宗族,特别是 PARP1 和 2 与 DNA 单链修正密切相关,所以 PARP 按捺剂对 BRCA1/2 有缺点的细胞有杀伤效果。
PDX1 操控胰腺的胚胎期发育,存在于正常老练胰腺的β细胞中,在部分胰腺切除后和胰腺炎时 PDX1 可在导管细胞内从头表达,大约 90% 胰腺癌是导管腺癌,所以胰腺癌干细胞或许坐落胰腺导管并表达 PDX1,在恶性转化中发挥效果。PDX1 主要在肿瘤滋润边际和搬运淋巴结中表达,与 TNM 分级、细胞增殖和下降生计有关。
ZIP4 是新的胰腺癌分子标志,它能够将锌转运入细胞,而 ZNT 宗族则可将锌导出细胞。锌是许多酶的辅佐因子,对高代谢和快速割裂的细胞很重要,如癌细胞。ZIP4 在大多数胰腺肿瘤中过度表达,或许与胰腺肿瘤开展相关。小鼠模型显现 ZIP4 缄默沉静下降肿瘤成长,过度表达促进肿瘤成长和搬运。
对 42 例胰腺癌安排选用 Sanger 测序,发现了 ZIP4 的改动,并判定了几处 SLC39A4 的 SNP,部分 SNP 坐落蛋白异构体 1 的发动子区域,或许会改动 ZIP4 表达。另只需一例胰腺癌安排存在蛋白异构体 1 密码子 459 和蛋白异构体 2 密码子 484 错义骤变,因为发作频度低,或许是布景骤变,还有几例肿瘤安排存在杂合性缺失(LOH)。
ZIP4 基因的错义片段或许会下降细胞对负性调理的反响,但需求功用剖析证明这一假说;每个 SNP 也都需求进一步研讨,建立其与蛋白功用的相关性。上述成果表明 SLC39A4 在胰腺肿瘤中骤变并不显着,ZIP4 野生型的过度表达或许有助于胰腺癌成长。
EUS-FNA 对评价胰腺癌是一项十分有远景的技能,这种技能侵袭性小,无需糟蹋很多资源,为遗传学和免疫组化检测供给标本。胰腺癌骤变发作很快,敏捷发生医治拮抗,而 EUS-FNA 能够实时供给标本进行遗传学改动研讨。联合 FNA 和遗传学查看或许会成为前期检测胰腺癌、优化医治的有远景的办法。
胰腺癌的药物基因组学
遗传学影响药物医治的相关常识有助于改进个体化医治的有用性。1997 年吉西他滨作为规范医治,同 5-氟脲嘧啶比较,能够改进痛苦操控和 OS。吉西他滨是胞嘧啶的类似物和前药,在体内转化为活性代谢物,阻挠 DNA 组成,但这种相互效果却能够因为 RECQL 基因的多态性而被打断,RECQL 基因编码 DNA 解螺旋酶,
吉西他滨进行活化代谢时必需穿过细胞膜并磷酸化,这个进程由 hENT 和 hCNT 核苷酸转运子完结。胰腺导管腺癌吉西他滨医治后选用免疫组化办法查看,具有可检测和不行检测的 hENT1 者,中位生计时刻分别为 13 个月和 4 个月,并且 hENT1 蛋白表达与辅佐性吉西他滨医治患者的 OS 和无病生计显着相关。
低水平 hENT1 的患者或许不会获益于吉西他滨医治,可是吉西他滨 5′-反式油酸,也称作 CO-1.01,或许是破例,该药是吉西他滨的脂肪酸衍生物,不需求 hENT1 转运其经过细胞膜。一项 II 期实验比较低表达 hENT1 患者对吉西他滨与 CO-1.01 的医治反响,研讨正在进行中。
清晰胰腺癌患者 hENT1 基因序列在临床上很有含义,因为一些亚组患者或许对吉西他滨更灵敏,只需较低剂量医治即可。判定 hENT1 发动子或外显子区域的骤变或许会清晰 hENT1 蛋白表达水平或功用状况的改动,并据此调整药物医治剂量。CO-1.01 能够作为医治的另一种挑选。
吉西他滨的代谢能影响其医治有用性,脱氧胞嘧啶激酶 (DCK) 和胞嘧啶核苷脱氨酶 (CDA) 影响医治有用性,因为 DCK 使吉西他滨磷酸化为活性方式,CDA 则将吉西他滨代谢为无活性方式。
研讨发现 DCK 低和高的胰腺癌患者 OS 分别为 14.6 和 21.7 个月,但 DCK 低者较高者至少年长 10 岁,阐明年纪相关甲基化和表观要素或许会影响 DCK 水平。对人类胰腺癌细胞株评价,发现 DCK 的 AG 基因型对吉西他滨灵敏性超越 GG 基因型,阐明 SNP 能够猜测吉西他滨有用性。一项 CDA 研讨发现患者具有纯合 CDA*3 时 CDA 活性特别低,吉西他滨医治发生严峻毒性。
FOLFIRINOX 联合 5-FU、伊立替康、亚叶酸和奥沙利铂是胰腺癌医治的一大开展,同单药吉西他滨比较,添加 IV 期疾病 OS 4.3 个月,但一起毒性也显着添加。FOLFIRINOX 计划中包含 5-FU,5-FU 的代谢机制或许会影响个体化医治。
二氢嘧啶脱氢酶(DPD)是担任 5-FU 代谢的要害酶,一项研讨中包含 II 期及以上胰腺癌,研讨 DPD 表达与 5-FU 肝脏灌注化疗间的联系及 OS,成果显现术后 5-FU 医治患者,DPD 水平低者较高者有生计获益。还有研讨归入 171 例患者,二处 DPD 的 SNPs,IVS14+1 G>A 和 2946 A>T 与 5-FU 前期医治毒性显着相关。总归基因组查看可猜测毒性、断定精准的有用化疗剂量。
药物运送的药物基因组学
胰腺肿瘤药物运送屏障包含过多的纤维安排和细密的基质,后者主要由排泄的酸性蛋白和富于半胱氨酸(SPARC)构成,SPARC 有多种功用,包含促进创伤愈合;经过调理基质堆积和转化、细胞粘附以及细胞外信号来介导细胞和微环境间的相互效果;还可按捺血管生成,参加上皮-间充质转化(EMT),诱导形状学改动丢掉粘附特性。
SPARC 在胰腺癌细胞株中或许是肿瘤按捺基因,因为 shRNA 按捺内源性 SPARC 能促进细胞成长,外源性 SPARC 按捺细胞成长和搬迁。附近原发胰腺肿瘤的基质纤维细胞表达高水平 SPARC,或许参加结缔安排构成、下降血管密度和细胞侵袭。SPARC 在附近纤维细胞的表达经过肿瘤-基质相互效果调理,也或许经过旁排泄调理,或许是为了操控侵袭性肿瘤成长而作出的反响。
探究 SPARC 在胰腺癌中的效果或许会改进胰腺癌医治形式。从正常安排到缓慢胰腺炎安排,到非恶性安排,直至胰腺癌,SPARC 基因甲基化(TRR)程度继续增高,已发现二个相对过度甲基化波峰,CpG 区域 1 和 CpG 区域 2。
正常胰腺中 CpG 区域 1 常常甲基化,而 CpG 区域 2 则很少甲基化,但在附近胰腺癌的非恶性安排中 CpG 区域 2 的甲基化水平显着高于正常胰腺安排,并且高 CpG 区域 2 甲基化与大肿瘤、烟草、喝酒、缓慢胰腺炎相关,所以有或许成为前期确诊胰腺肿瘤的标志。
另一个 SPARC 的检测办法是 FNA 活检,进行安排 mRNA 剖析,这个办法很重要,因为不是一切的 FNA 标本都足够大、合适免疫组化查看。有研讨发现 SPARC mRNA 高水平表达是显着的胰腺癌独立预后标志,低水平 SPARC mRNA 的胰腺癌 5 年生计率为 20.24%,而高水平 SPARC mRNA 的患者 5 年生计率为 0。
以往的研讨探讨了 SPARC 在运送药物中的效果,并比较了白蛋白紫杉醇联合吉西他滨与单药吉西他滨的效果,成果显现白蛋白紫杉醇能添加肿瘤内吉西他滨的浓度,削减肿瘤周围纤维间质,这意味着白蛋白紫杉醇或许靶向基质 SPARC 并答应化疗药物运送进入肿瘤。SPARC 对胰腺癌的效果仍不清楚,需求进一步研讨其靶向胰腺癌医治的潜能。
按捺 SPARC 表达或许会阻挠胰腺癌经过 p53 诱导的核蛋白 1(TP53INP1)进行的侵袭,TP53INP1 能上调 p53 并在体外减低细胞搬迁。胰腺癌中它的表达缺失,而康复表达后则可按捺胰腺肿瘤开展,胰腺癌细胞显现 TP53INP1 表达缺失者具有高度搬运性。
正常胰腺中 miR-155 很低,答应 TP53INP1 按捺 SPARC 表达,并削减细胞搬迁。在 PanIN l 危害中,高水平 miR-155 能下调 TP53INP1 并上调 SPARC,添加细胞搬迁。胰腺癌中 miR-155 水平很高,TP53INP1 彻底阻滞,一起 SPARC 发动子过度甲基化,但胰腺癌细胞搬迁才能仍有添加,是因为基质细胞过表达 SPARC。
其它与胰腺癌有关的几个基因如 SLC39A4 和 PDX1 等,有促进胰腺癌成长的效果。胰腺癌中 ZIP4 在杂乱的信号网络中发挥效果,如 miRNAs、细胞因子和锌依靠转录因子,小鼠胰腺癌模型中经过 RNA 搅扰下调 ZIP4 发挥肿瘤按捺效果,靶向这些下流效应子的医治或许会成为新的有用医治胰腺癌的办法。
PDX1 也显现出医治胰腺癌、胰岛瘤和胰岛恶性肿瘤的效果。特别规划的 RNA 搅扰效应子渠道,是具有生物功用的 shRNAPDX-1 脂质体复合物,能敏捷下降小鼠胰腺癌异种移植模型的肿瘤容积、添加生计。需求进一步清晰,依据胰腺癌中 ZIP4 和 PDX-1 的改动进行的靶向医治的安全性和有用性。
总结
基因组测序具有改进胰腺癌确诊与医治的巨大潜能。近期遗传学研讨清晰了一些胰腺癌新的标志和医治靶点,可是现有查看办法实践性不强。因为胰腺癌远期预后差,判定其遗传学改动的需求十分火急,发现新的胰腺癌遗传学改动对改进胰腺癌的确诊、药物剂量的精确性及发现新的医治手法十分有协助。
 当代健康
当代健康